Clorometilación de Blanc
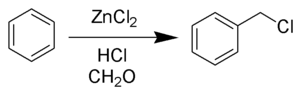
La Clorometilación de Blanc o Reacción de Blanc es una reacción orgánica de anillos aromáticos que utiliza formaldehído y ácido clorhídrico catalizados por cloruro de zinc u otro ácido de Lewis para formar clorometil arenos.[1][2] Fue desarrollada por el químico francés Gustave Louis Blanc (1872-1927).[3][4][5] La reacción se realiza con cuidado ya que, como la mayoría de las reacciones de clorometilación, produce un bis(clorometil) éter altamente cancerígeno como subproducto.
Mecanismo[editar]
La reacción se realiza en condiciones ácidas y con un catalizador ZnCl2. Estas condiciones protonan el formaldehído carbonilo haciendo que el carbono sea mucho más electrofílico. El aldehído es entonces atacado por los pi-electrones aromáticos, seguido por la rearomatización del anillo aromático. El alcohol bencílico así formado se convierte rápidamente en cloruro en las condiciones de reacción.
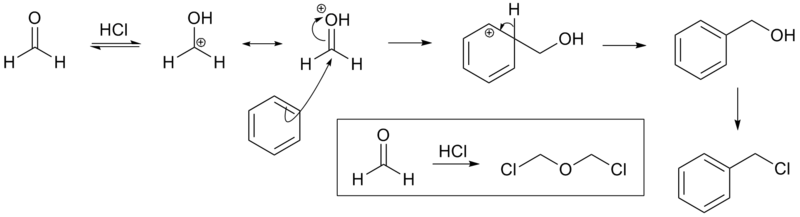
Aunque la reacción es un medio eficaz para introducir un grupo clorometil, la producción de pequeñas cantidades de bis(clorometil) éter altamente cancerígeno es una desventaja.
Clorometilados relacionados[editar]
La clorometilación de tioles puede realizarse con HCl concentrado y formaldehído:[6]
- ArSH + CH2O + HCl → ArSCH2Cl + H2O
La clorometilación también puede realizarse utilizando
- ArH + CH3OCH2Cl → ArCH2Cl + CH3OH
Esta reacción se emplea en la clorometilación de estireno en la producción de resinas de intercambio iónico y resinas de Merrifield.[7]
Véase también[editar]
- Organic chemistry portal: Blanc reaction [1]
- Alquilación de Friedel-Crafts
- Reacción de Quelet
Referencias[editar]
- ↑ Gustave Louis Blanc Bull. Soc. Chim. France 1923, 33, 313.
- ↑ Fuson, R. C.; McKeever, C. H. Org. React. 1942, 1, 63. (Review).
- ↑ Gustave Louis Blanc Bull. Soc. Chim. France 1923, 33, 313
- ↑ Whitmore, F. C.; Ginsburg, Abram; Rueggeberg, Walter; Tharp, I.; Nottorf, H.; Cannon, M.; Carnahan, F.; Cryder, D.; FLeming, G.; Goldberg, G.; Haggard, H.; Herr, C.; Hoover, T.; Lovell, H.; Mraz, R.; Noll, C.; Oakwood, T.; Patterson, H.; Van Strien, R.; Walter, R.; Zook, H.; Wagner, R.; Weisgerber, C.; Wilkins, J. (May 1946). «Production of Benzyl Chloride by Chloromethylation of Benzene. Laboratory and Pilot Plant Studies». Industrial & Engineering Chemistry 38 (5): 478-485. doi:10.1021/ie50437a013.
- ↑ Belen'kii, Leonid I; Vol'kenshtein, Yu B; Karmanova, I B (30 de septiembre de 1977). «New Data on the Chloromethylation of Aromatic and Heteroaromatic Compounds». Russian Chemical Reviews 46 (9): 891-903. Bibcode:1977RuCRv..46..891B. doi:10.1070/RC1977v046n09ABEH002180.
- ↑ D. Enders, S. Von Berg, B. Jandeleit (2002). «Diethyl [(Phenylsulfonyl)methyl]phosphonate». Org. Synth. 78: 169. doi:10.15227/orgsyn.078.0169.
- ↑ François Dardel and Thomas V. Arden "Ion Exchangers" in Ullmann's Encyclopedia of Industrial Chemistry, 2008, Wiley-VCH, Weinheim. doi 10.1002/14356007.a14_393.pub2
